専門獣医師が解説するウサギの検疫対象三大疾患(兎粘液腫)

目次
ウイルスによる腫瘍
兎粘液腫(うさぎねんえきしゅ)とはポックス科レポリポックスウイルス属のウサギミクソーマウイルス(ウサギ粘液腫ウイルス)の感染で起こる腫瘍疾患です。感染するとウサギへの被害が大きく、日本では家畜伝染病予防法における届出伝染病に指定され、そのために海外からウサギを輸入する場合などは、空港や港において、検疫が行われています。日本での発生は稀に報告されています。
ウサギ粘液腫ウイルスの株
粘液腫ウイルスは病原性が異なる様々な株が存在します。アメリカ西海岸とメキシコ固有のカリフォルニア株が最も毒性が高く、致死率は100%と報告されています。南アメリカと中央アメリカの南アメリカ菌は、わずかに毒性が低く、99.8%の致死率が報告されています。ヨーロッパとオーストラリアに存在の株は弱毒化しており、致死率は50〜95%と報告され、ヨーロッパとオーストラリアの野生のウサギはウイルスに対する免疫をある程度発達させましたが、一般的にペットのウサギには免疫は獲得していません〔Kerr 2017〕。
全てのウサギで起こるの?
粘液腫ウイルスの自然宿主は、中南米ではモリウサギ、北米ではブラシウサギですが、これらのウサギはウイルスに対する免疫を持っており、感染した部位が一時的に腫れるだけの軽度の症状しか見られません。同じく南米および北米に棲息するワタオウサギ属のウサギでも流行していましたが、やはり症状が軽いです。しかしながら、ペットのウサギのオリジナルであるヨーロッパアナウサギでは重度で通常は致命的な病気を引き起こします〔Kerr 2017〕。イギリスでは稀にヤブノウサギやユキウサギに感染することもありましたが、その個体数に与える影響はほとんどありませんでした〔Kerr 2013〕。粘液腫症は、ウイルスが適応した特有のウサギでは症状が軽度ですが、他の種類のウサギに感染すると重症化するという特徴があります。

アナウサギの症状
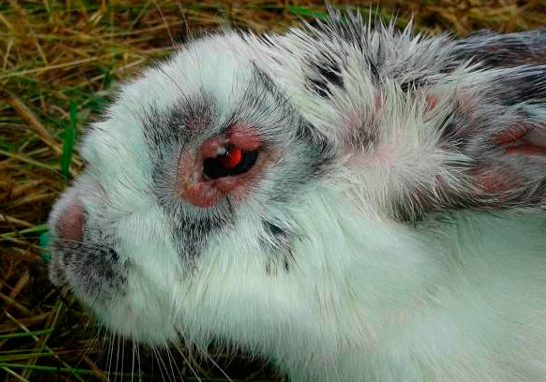
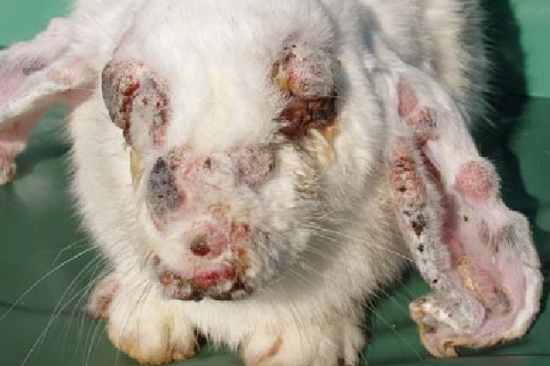
ウイルスに感染したウサギは、感染から1週間以内に発症します。数日後には眼瞼や鼻、耳、肛門、生殖器などがゼラチン様の腫脹を起こし。目も開けられず、耳も聞こえない状態となり、その特徴的な外貌からライオンフェイス(Rion face)と呼ばれています。粘液膿性の鼻汁も見られ、呼吸困難もなります。発熱、嗜眠や沈鬱、食欲不振も起こして、細菌の二次感染による肺炎や多臓器不全が起こり、感染後約2週で死亡する例が多いです。ウイルスの株やウサギの免疫状態に依存し、南米や北米に存在するような毒性の高い株での感染では、感染から数日以内に死亡し、弱毒化された株の感染では皮膚病変のみが見られ、支持療法で延命します。
kroliki.pp.ua/міксоматоз-кролів-лікування/
https://www.abbeyvetspets.co.uk/wp-content/uploads/2018/08/myxo.png
ヨーロッパアナウサギが南米の粘液腫ウイルス株の皮内注射を受けた実験では、接種後約2日で接種近くのリンパ節にウイルスが発見され、3日目には血流と腹部の臓器にウイルスが発見されました。約4日で、ウイルスは接種されていない皮膚および試験から分離されました。 5日目に眼瞼のわずかな肥厚と結膜液中のウイルスの存在が検出され、6日目に精巣に充血が認められました〔Fenner et al.1953〕。
診断したら届出
粘液腫症の診断は、特徴的な臨床的外観に基づいて行われることがよくあります。届出伝染病であるため、典型的な症状を示した場合、あるいはウサギが死亡した場合は、獣医師は保健所に届け出をするべきです。
感染経路は?
粘液腫ウイルスは主に、ノミ(ウサギノミ)、ダニ、シラミ、ハエなどによって媒介されます。一般的にの昆虫や節足動物の咬傷を介して発生し、これらの動物が活動的になる春~夏に多発します〔Kerr 2017〕。また、直接接触することによっても感染することも示唆され、感染したウサギの眼や鼻の分泌物や侵食された皮膚からウイルスを排出し、ウイルスは精液や生殖器の分泌物にも存在しています。粘液腫ウイルスは環境中でかなり安定しており、ケージ、エサ入れや給水器、人の手などの汚染された物によって蔓延する可能性があります〔Kerr 2017〕
治療できるの?
現在、粘液腫症に対する特定の治療法はありません。
予防
予防は消毒とワクチン、そして媒介生物の接触予防になります。
消毒
粘液腫ウイルスは乾燥に耐性があります〔Disinfection 2019〕。消毒は、塩素系、水酸化ナトリウやホルマリンが推奨されています〔Oglesbee et al.2011〕。
マイクロシンAH マイクロシンクリーナー 1L
楽天購入コチラ!
コレ最高!ケージや小屋を消毒して!マイクロシンクリーナーは最先端特許技術によりウイルス、細菌、真菌(カビ)を瞬時に阻害し、清潔な状態にしてくれます。おまけに動物や糞・オシッコの嫌な臭いまで除去します。 医療機関や動物病院の病室やICU、手術室などで使用されている優れ物です!
ワクチン
粘液腫症のワクチンは、いくつかの国で使用されていますが、日本にはありません。兎粘液腫症とウサギ出血性疾患の両方を予防するワクチンが使用されています〔Nobivac Myxo RHD Data Sheet 2019〕。
https://www.vettimes.co.uk/news/msd-launches-nobivac-myxo-rhd/
ノミやダニの予防
ワクチンは100%の防御を提供しませんので、野生のウサギやノミやダニ・昆虫などの媒介動物との接触を防ぐことは重要です。
ウイルスによるウサギ退治/ウイルスの弱毒化と抗体免疫獲得
オーストラリアとヨーロッパのアナウサギに対して個体数増加を押さえるため粘液腫ウイルスを戦略的に拡散さていたことがありました。その結果、粘液腫症抵抗性のウサギの増加と弱毒化したウイルス変異体が出現し、ウイルスの宿主-病原体の共進化を招いた、戦略の失敗の例になりました〔MacLachlan 2017〕。
オーストラリア
ヨーロッパのウサギは、18世紀にオーストラリアに食料源として持ち込まれました。しかし、野生のウサギの個体数は、オーストラリアでは作物に数百万ドルの損害を与える害獣と変貌してしまいました。そこでウサギの個体数を制御するために、20世紀に様々な方法が試みられてきました。射撃と巣穴からの確保から始まり、1907年にはウサギに強いフェンスを建設して、ウサギを封じ込めようとしましたが、これも失敗しました〔Broomhall 1991〕。1950年代にウサギ粘液腫症を引き起こす粘液腫ウイルスを、野生に散乱させることで個体数を大幅に減らす効果がありました。しかし、その後、粘液腫症抵抗性のウサギの増加と弱毒化ウイルス変異体が出現して、個体数が回復するようになりました。1995年以来には、ウサギ出血性疾患ウイルスが個体数を制御するためにも使用されています〔Mahar et al.2018〕。
ヨーロッパ
1952年フランスでは2頭の野生のウサギに粘液腫ウイルスを接種して根絶をはかり、ウイルスはすぐに西ヨーロッパ、アイルランド、イギリスに蔓延しました〔Kerr et al.2015,Bartrip 2008〕。その結果、ウサギは根絶に近い状態になりましたが、ウサギを補食するイベリアオオヤマネコやイベリアカタシロハシなどの捕食者が絶滅の危機に瀕しました〔Gil-Sánchez et al.2011,Sánchez .2019〕。そして、野生のウサギだけでなく、肉や毛皮用の家兎を生産する大規模なウサギの飼育産業にも大きな影響を及ぼしました。最終的にはオーストラリアと同様に免疫を獲得したウサギの増加と弱毒化ウイルス株の出現により、激減は歯止めがかかりました〔Kerr et al.2015〕。
ウサギを医学的に勉強するならこの本!
ウサギの病気や治療のことも知りたい方は、これを読んで下さい!ウサギ診察獣医師のバイブルです!
JCRA(ジャクラ)って?ウサギ検定受けませんか?
ウサギを幸せに長生きさせたい方は、一般社団法人 日本コンパニオンラビット協会(JCRA)に入会て、ウサギ検定を受験しましょう!
参考文献
■Bartrip P.Myxomatosis:A History of Pest Control and the Rabbit.Tauris Academic Studies.London.UK.2008
■Broomhall FH.The longest fence in the world:a history of the no.1 rabbit proof fence from its beginning until recent times.Hesperian Press.Carlisle.WA.1991
■Disinfection.The Center for Food Security and Public Health.Retrieved21.2019
■Fenner F,Woodroofe GM.The pathogenesis of infectious myxomatosis: the mechanism of infection and the immunological response in the European rabbit(Oryctolagus cuniculus).The British Journal of Experimental Pathology34(4).400–411.1953
■Gil-Sánchez JM,McCain EB.Former range and decline of the Iberian lynx(Lynx pardinus) reconstructed using verified records.Journal of Mammalogy92(5).1081–1090.2011
■Kerr P.Genomic and phenotypic characterization of myxoma virus from Great Britain reveals multiple evolutionary pathways distinct from those in Australia. PLOS Pathogens13(3).e1006252.2017
■ Kerr P.Viral Infections of Rabbits.Veterinary Clinics of North America: Exotic Animal Practice16(2).437–468.2013
■Kerr P,Liu J,Cattadori I et al.Myxoma Virus and the Leporipoxviruses:An Evolutionary Paradigm.Viruses7(3).1020–1061.2015
■MacLachlan J.Fenner’s Veterinary Virology.5th ed.Elsevier.p168.2017
■Meredith A.Viral skin diseases of the rabbit.Veterinary Clinics of North America:Exotic Animal Practice16(3).705–714.2013
■Nobivac Myxo RHD Data Sheet.European Medicine Agency.Retrieved20.2019
■Oglesbee, B.Blackwell’s Five-Minute Veterinary Consult:Small Mammal(Second ed.). West Sussex, UK:Wiley-Blackwell.p455.2011.
■Rabbits around a waterhole at the enclosed trial site at Wardang Island, 1938.National Archives of Australia.Retrieved28.2019
■Sánchez B.Action plan for the Spanish imperial eagle (Aquila adalberti) in the European Union.European Commission.Retrieved14.2019
■Mahar JE,Read AJ,Gu X,Urakova N,Mourant R,Piper M,Haboury S,Holmes EC,Strive T,Hall RN. Detection and Circulation of a Novel Rabbit Hemorrhagic Disease Virus in Australia.Emerg Infect Dis24(1).22–31.2018
![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/2607a2df.171c83f3.2607a2e0.a88bf243/?me_id=1391393&item_id=10002004&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fpetlovers%2Fcabinet%2F08571982%2Fdo660.jpg%3F_ex%3D128x128&s=128x128&t=picttext)
![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/26090119.dfc29016.2609011a.dd08dc4f/?me_id=1367504&item_id=10734737&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fmifsoft%2Fcabinet%2Fb%2F3%2F391%2F9784895313391.jpg%3F_ex%3D128x128&s=128x128&t=picttext)